Neuroelectrics anunció hoy que la FDA ha aprobado el estudio de protocolo suplementario de Exención de Dispositivos en Investigación presentado por Neuroelectrics para ayudar a los pacientes con Trastorno de Depresión Mayor (MDD)
La pandemia de COVID-19 ha puesto de manifiesto la necesidad urgente de una intervención segura, eficaz y basada en el hogar para los pacientes que sufren un episodio de MDD.
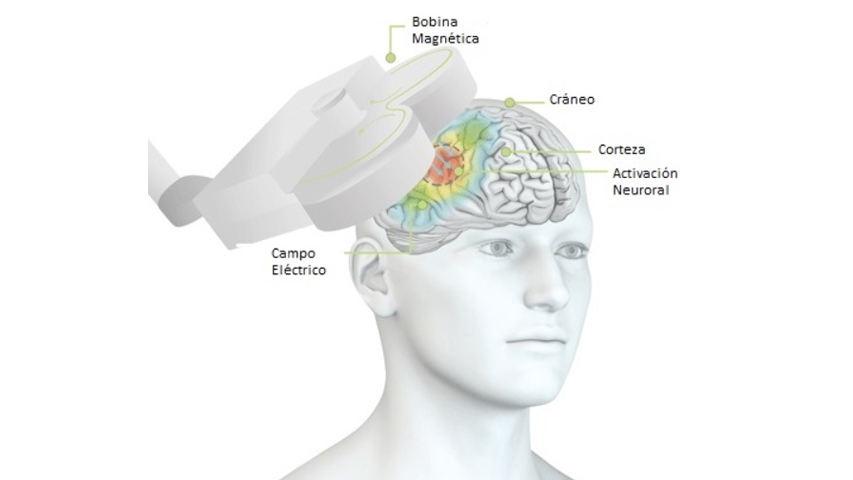
La estimulación transcraneal de corriente continua (tDCS) se está investigando para poder proporcionar una solución adecuada. Neuroelectrics propuso un estudio de telesalud aprovechando su sistema único basado en el hogar que permite un tDCS supervisado y entregado por el cuidador para pacientes con MDD que no pueden acceder a su tratamiento actual debido a las restricciones de la pandemia.
El objetivo principal del estudio es satisfacer las necesidades médicas de los pacientes proporcionando una intervención de tDCS en el hogar a las personas que son candidatas adecuadas para rTMS o ECT pero que no pueden acceder a estas terapias debido a la pandemia de COVID-19.
El estudio también permitirá evaluar la eficacia, la aceptabilidad y el cumplimiento del tratamiento del sistema de tDCS basado en el hogar de Neuroelectrics para pacientes con MDD.

El investigador principal del estudio será Alvaro Pascual-Leone, MD, PhD, profesor de neurología de la Escuela de Medicina de Harvard; científico senior, Hinda y Arthur Marcus Institute for Aging Research, Hebrew SeniorLife.
El trastorno depresivo mayor (TDM) es muy prevalente y la principal causa de discapacidad mundial en todo el mundo.
Alrededor del 20-40 % de los pacientes no se benefician lo suficiente de las intervenciones antidepresivas existentes, incluidos los ensayos de medicación y psicoterapia (Greden, 2001). Los tratamientos farmacológicos tienen una eficacia limitada, los efectos secundarios son comunes (Carvalho et al., 2016) y un tercio de los pacientes son resistentes a los medicamentos que no logran la remisión después de usar tres o más antidepresivos (Rush et al., 2006) y experimentan episodios depresivos recurrentes. (Nemeroff, 2007).
Fundado en 2012, el sistema Neuroelectrics EEG (Enobio) recibió la autorización 510K de la FDA de EE. UU. en mayo de 2017.
Neuroelectrics está investigando actualmente una nueva plataforma para proporcionar nuevas terapias cerebrales personalizadas para pacientes con trastornos cerebrales utilizando estimulación cerebral no invasiva. La tecnología única y patentada monitorea la actividad eléctrica del cerebro (EEG) y estimula (tES) las regiones o redes cerebrales con corrientes eléctricas suaves. La empresa está entrando en una fase fundamental para su producto de estimulación Starstim para la terapia de la epilepsia resistente al tratamiento.
“Estamos agradecidos a la FDA por su rápida reacción en tiempos de COVID, como empresa estamos listos para llevar nuestra plataforma a casa de los pacientes. Ahora más que nunca se necesita telemedicina, monitoreo cerebral y estimulación cerebral en el hogar, especialmente para los pacientes mayores que tienen aún más desafíos y restricciones para acceder a los entornos clínicos u hospitalarios”.
Ana Maiques, CEO de Neuroelectrics